Guía de uso
Reconstitución de péptidos liofilizados: la matemática concreta
Para 5mg en 2ml de BAC: concentración = 2.5 mg/ml = 2500 mcg/ml. La matemática de reconstitución es la garantía contra errores de dosis de un factor 10.
~8 min de lectura Revisado: evidencia robusta
Por Redacción Peptilab 24 de marzo de 2026
Cómo reconstituir péptidos de investigación paso a paso: agua bacteriostática, concentración mg/ml, aritmética de dosis por unidad de jeringa, errores comunes.

En este artículo (13 secciones)
Esta guía explica cómo reconstituir péptidos liofilizados con la aritmética exacta que se usa en protocolos de investigación. Nada aquí es consejo médico; es matemática de laboratorio y procedimiento estándar de manipulación de reactivos.
Qué es la reconstitución
Los péptidos de investigación se entregan liofilizados (freeze-dried): un polvo blanco o amarillo pálido al fondo del vial, resultado de eliminar agua por sublimación. Esta forma es estable durante meses a temperatura de refrigeración. Para usar el compuesto en protocolos inyectables, se debe reconstituir: disolver el polvo en un diluyente estéril hasta obtener una solución clara a una concentración conocida.
El diluyente estándar es agua bacteriostática: agua estéril con 0.9% de alcohol bencílico como conservante. El alcohol bencílico mantiene la esterilidad durante múltiples extracciones del mismo vial durante 28 días a 2–8°C. Esto es crítico: una solución reconstituida con agua estéril sin conservante solo es apta para uso único por esterilidad.
La aritmética básica: mg, ml, mcg, unidades
Hay cuatro unidades que intervienen:
- mg (miligramo): cantidad total de péptido en el vial liofilizado. Ejemplo: 10mg.
- ml (mililitro): volumen de agua bacteriostática añadido. Ejemplo: 1ml o 2ml.
- mg/ml: concentración resultante. 10mg / 1ml = 10mg/ml.
- mcg (microgramo): dosis individual. 1mg = 1,000mcg.
- unidad: graduación de la jeringa de insulina. Una U-100 (la más común) tiene 100 unidades por 1ml, por lo que cada unidad = 0.01ml.
Ejemplo trabajado completo:
- Vial: 10mg de Tirzepatida.
- Diluyente: 1ml de agua bacteriostática.
- Concentración: 10mg/ml = 10,000 mcg/ml.
- Jeringa: U-100 (1 unidad = 0.01ml).
- Por unidad de jeringa: 10,000 mcg/ml × 0.01 ml = 100 mcg por unidad.
- Si la dosis objetivo del protocolo es 5mg (5,000 mcg): 5,000 / 100 = 50 unidades de jeringa.
Para automatizar esto y evitar errores, hay una calculadora de dosis mcg que hace el cálculo para cualquier combinación de vial / agua / jeringa / dosis objetivo.
Volumen de reconstitución: más o menos agua
La misma cantidad de péptido se puede reconstituir en distintos volúmenes, obteniendo distintas concentraciones:
| Vial | Agua | Concentración | mcg/unidad (U-100) |
|---|---|---|---|
| 10mg | 1ml | 10mg/ml | 100 |
| 10mg | 2ml | 5mg/ml | 50 |
| 10mg | 2.5ml | 4mg/ml | 40 |
| 10mg | 5ml | 2mg/ml | 20 |
¿Por qué variar? Dos razones:
- Precisión en dosis bajas: si la dosis objetivo es 250 mcg, con 100mcg/unidad son 2.5 unidades (difícil de leer con precisión). Con 20 mcg/unidad son 12.5 unidades (mucho más preciso).
- Espacio en la jeringa: una dosis de 5,000 mcg a 100 mcg/unidad son 50 unidades (cabe en jeringa de 0.5ml). La misma dosis a 20 mcg/unidad son 250 unidades (excede la capacidad de una jeringa de 1ml). Hay que elegir concentración acorde a la dosis típica del protocolo.
Regla general: protocolos de Tirzepatida / Retatrutida (dosis en rango de 2.5mg a 15mg) → concentración alta (10mg/ml con 1ml). Protocolos de BPC-157 / TB-500 (dosis en rango de 250–500 mcg) → concentración más baja (5mg/ml con 2ml).
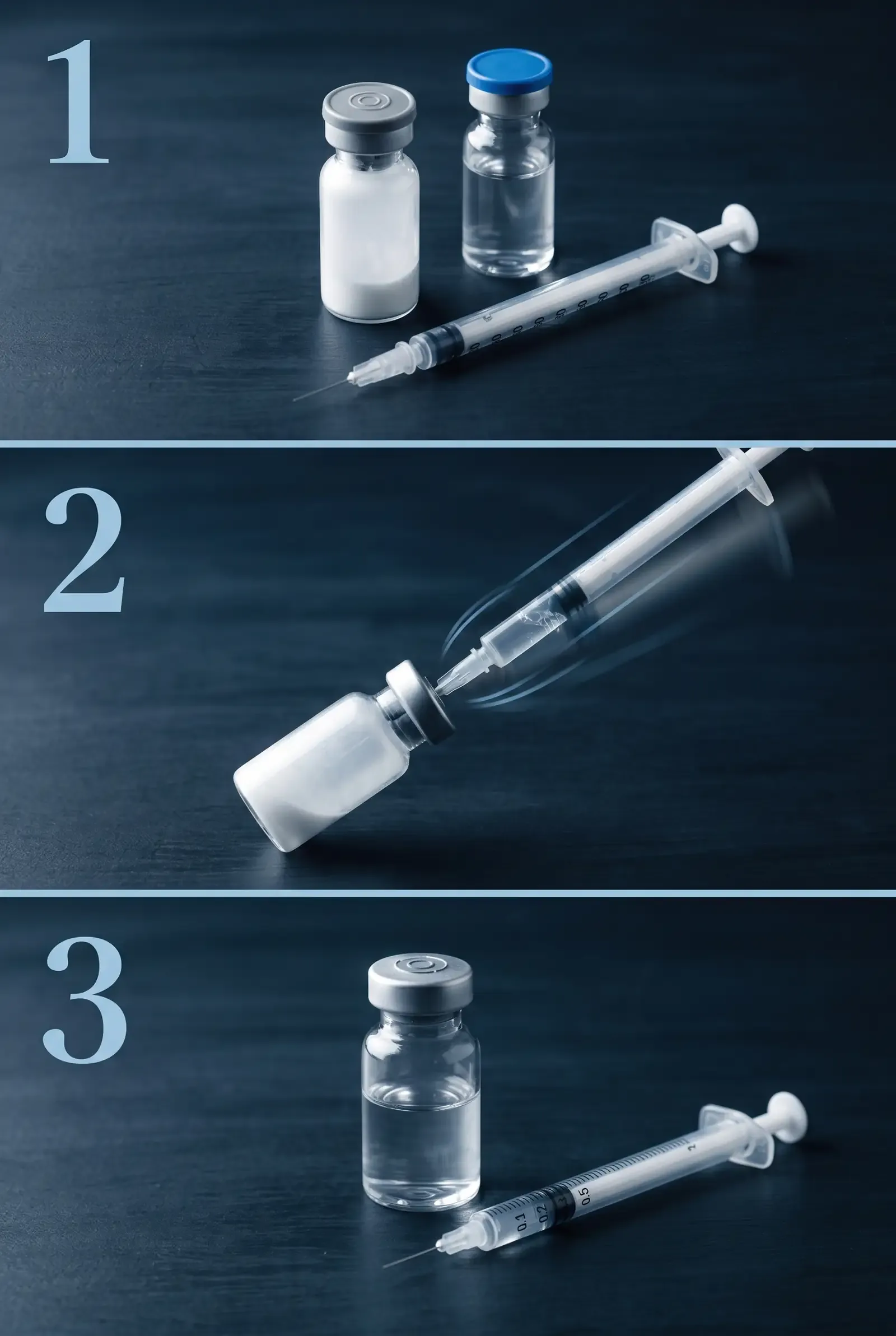
Los tres pasos clave: materiales, transferencia, y solución lista. El procedimiento detallado está abajo.
Procedimiento paso a paso
- Llevar los viales a temperatura ambiente (15–20 minutos). Inyectar agua fría en polvo frío puede causar nebulización.
- Limpiar los tapones de goma de ambos viales (péptido y agua bacteriostática) con torunda de alcohol isopropílico al 70%. Dejar secar 10 segundos.
- Aspirar el volumen de agua con una jeringa apropiada. Para 1ml, usar jeringa de 1ml (no la de insulina U-100, que es incómoda para aspirar volumen).
- Inyectar el agua por el costado interno del vial del péptido, apuntando al cristal lateral, no directamente sobre el polvo. El chorro directo puede desnaturalizar algunos péptidos.
- Girar suavemente hasta disolver. No agitar. La agitación mecánica de soluciones peptídicas puede causar denaturación y formación de agregados. La disolución debe tomar de 30 segundos a 2 minutos.
- Verificar apariencia: solución clara, incolora. Cualquier turbidez, partícula visible o color anómalo implica que el vial no se usa y se descarta.
- Etiquetar el vial con la fecha de reconstitución. Estabilidad típica: 28 días a 2–8°C. No congelar tras reconstituir.
Errores comunes y cómo evitarlos
Error 1: confundir ml con unidades. 1ml son 100 unidades en U-100. Aspirar “10 unidades” cuando el protocolo dice “0.1ml” es lo mismo; aspirar “10ml” cuando el protocolo dice “0.1ml” es 100 veces la dosis.
Error 2: confundir mg con mcg. 1mg = 1,000mcg. Inyectar “5mg” cuando el protocolo dice “5mcg” es 1,000 veces la dosis. La calculadora de dosis convierte esto automáticamente, pero conviene entender la aritmética base.
Error 3: no considerar volumen muerto de la jeringa. Las jeringas de insulina tienen ~0.05ml de volumen que queda en la aguja y el cono después de inyectar. En dosis pequeñas, esto representa un error porcentual significativo. Para dosis sub-1-unidad, se recomienda usar jeringas con aguja fija (menor volumen muerto).
Error 4: reconstituir con agua estéril en lugar de bacteriostática. Agua estéril sin conservante solo es apta para uso único por esterilidad. Usar agua estéril por descuido y seguir extrayendo del mismo vial durante días implica riesgo microbiológico.
Error 5: agitar el vial. Los péptidos son moléculas delicadas. Agitar vigorosamente puede causar pérdida de potencia por denaturación. Girar suavemente siempre.
Estabilidad post-reconstitución
Los compuestos peptídicos de investigación tienen estabilidad post-reconstitución variable:
- Tirzepatida, Retatrutida, Semaglutida, Cagrilintida: hasta 28 días a 2–8°C.
- BPC-157, TB-500: hasta 30 días a 2–8°C.
- GHK-Cu: hasta 30 días a 2–8°C con protección de luz (el vial debe guardarse en la caja o envuelto).
- Epithalon: hasta 28 días a 2–8°C.
Nunca congelar péptidos reconstituidos. El ciclo de congelación-descongelación degrada la estructura secundaria y reduce la actividad. Para almacenamiento prolongado, el vial liofilizado sin reconstituir es la opción correcta (estabilidad de meses a temperatura de refrigeración).

Qué necesitas antes de reconstituir
- El vial de péptido liofilizado con su COA verificado.
- Un vial de agua bacteriostática de 3ml o 10ml.
- Jeringas de insulina U-100 (Farmatodo o droguerías en Colombia).
- Torundas de alcohol isopropílico al 70%.
- Opcional: jeringa de 1ml con aguja no insulina para aspirar el volumen de agua.
La aritmética correcta es la base. Si se equivoca en un factor 10, se equivoca en un factor 10 en cada dosis del protocolo. Por eso Peptilab provee la calculadora de dosis mcg como herramienta independiente: es el paso donde más frecuentemente ocurren errores evitables.
Preguntas frecuentes
¿Cómo calcular la dosis al reconstituir un péptido liofilizado?
Tres pasos: (1) Concentración = mg en el vial / ml de agua bacteriostática añadida. Ej: vial 10mg + 2ml agua = 5 mg/ml. (2) Conversión a mcg/ml = mg/ml × 1.000. Ej: 5 mg/ml = 5.000 mcg/ml. (3) Volumen de dosis = mcg deseados / mcg por ml. Ej: para 250 mcg → 250/5.000 = 0.05 ml = 5 IU en jeringa U-100. Regla práctica: 1 IU U-100 = 0.01 ml.
¿Cuántos ml de agua bacteriostática añadir a cada vial?
Depende del compuesto y dosis objetivo: GLP-1 (Tirzepatida, Semaglutida, Retatrutida): 1 ml para concentración 10 mg/ml (dosis altas, fácil escalada). BPC-157, TB-500: 2 ml para 5 mg/ml (dosis pequeñas, mejor precisión). GHK-Cu: 5 ml para concentración baja (dosis típicamente 1–5 mg). La convención facilita lectura en U-100; ajustar según protocolo específico.
¿Qué pasa si añado demasiada o muy poca agua al reconstituir?
Demasiada agua: concentración baja, dosis pequeña requiere volumen alto difícil de medir en U-100 (errores >5%). Muy poca agua: concentración alta, dosis pequeña en volumen menor a 0.02 ml difícil de aspirar sin pérdida en aguja. La actividad del péptido no se ve afectada por la cantidad de agua dentro del rango habitual (1–5 ml para viales 5–10 mg). El error es operacional, no farmacológico.
¿Por qué el vial tiene burbujas después de reconstituir?
Las burbujas son aire atrapado durante la inyección de agua bacteriostática. No afectan actividad del péptido. Esperar 5–10 minutos a temperatura ambiente o tocar suave el vial las disipa. Evitar agitación vigorosa (vórtex, sacudir): puede generar espuma persistente que indica desnaturalización proteica local. Inversión suave 3–5 veces es suficiente para mezclar.
¿Se puede reconstituir un vial parcialmente y guardar el resto seco?
No. Una vez añadida agua al vial, la totalidad del polvo se hidrata por difusión en minutos; no es posible reconstituir ‘solo una porción’. Si se anticipa uso lento (>30 días), considerar alicuotar post-reconstitución: dividir el volumen en viales estériles más pequeños y congelar (-20°C) las alícuotas no usadas inmediatamente. Estabilidad congelada reportada: >6 meses para mayoría de péptidos lineales.
Para investigación con material RUO documentado, ver el catálogo en /tienda/ o consultar por WhatsApp (respuesta < 2h hábiles).
Metodología de investigación
Lee también
Herramientas
Fuentes
Cómo se produjo este artículo
Equipo editorial de Peptilab.co. Cada análisis pasa por verificación Zero-Trust: toda cifra clínica enlaza a un ensayo publicado (NEJM, JAMA, NCT, comunicado oficial del fabricante). Si no hay fuente primaria verificable, el dato no se publica. Contenido de referencia para investigación científica (RUO), no recomendación médica.
- Estándares editoriales
- 1 fuente citada
- Actualizado:
¿Dudas o quieres consultar stock?
Nuestro equipo responde consultas por WhatsApp dentro de las 2 horas hábiles. Sin compromiso.